Studi Kasus – Epigenetika
- Materi 1: Regulasi Ekspresi Gen dan Epigenetika
- Materi 2 : Kontrol Pembelahan Sel dan Epigenetika
Studi Kasus Materi 1
- Kasus 1
- Kasus 2
- Kasus 3
- Kasus 4
- Kasus 5
- Kasus 6
Kasus 1 : Hipermetilasi dan Kanker Kolon
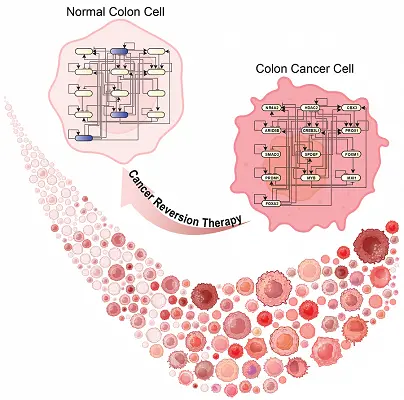
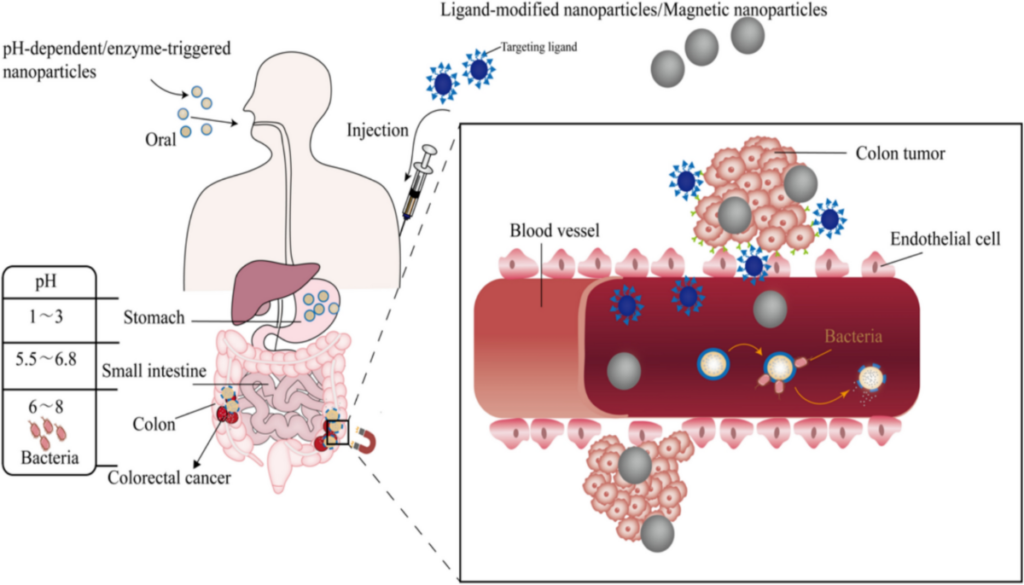
Seorang pria berusia 45 tahun didiagnosis menderita kanker kolon. Hasil pemeriksaan laboratorium menunjukkan bahwa ia tidak memiliki mutasi pada gen supresor tumor p16. Artinya, urutan DNA gen tersebut tetap normal.
Namun, ketika dilakukan analisis epigenetik, ditemukan bahwa bagian promoter gen p16 mengalami hipermetilasi (penambahan gugus metil dalam jumlah tinggi).
Akibatnya, gen p16 tidak dapat ditranskripsi dan tidak menghasilkan protein penghambat siklus sel. Tanpa protein ini, sel-sel di kolon membelah secara tidak terkendali dan berkembang menjadi kanker.
Konsep dasar:
Gen p16 (juga dikenal sebagai p16INK4a, CDKN2A, atau MTS1) adalah gen supresor tumor yang sangat penting dalam mengatur siklus sel. Terletak pada kromosom 9p21, gen ini berfungsi sebagai “rem” untuk mencegah pembelahan sel yang tidak terkendali.
Fungsi Utama p16
- Penghambat Siklus Sel: p16 bekerja dengan cara mengikat dan menghambat enzim CDK4 dan CDK6. Normalnya, enzim-enzim ini memicu sel untuk masuk ke fase pembelahan (fase S). Dengan menghambatnya, p16 menjaga sel tetap berada di fase istirahat (G1).
- Mengaktifkan Jalur Retinoblastoma (Rb): Dengan menghalangi CDK4/6, p16 menjaga protein Rb dalam bentuk aktif. Protein Rb yang aktif ini berfungsi mengunci faktor transkripsi E2F, sehingga gen yang dibutuhkan untuk replikasi DNA tidak bisa diaktifkan.
- Induksi Penuaan Sel (Senescence): p16 membantu memicu senescence, yaitu kondisi di mana sel berhenti membelah secara permanen namun tetap hidup, yang berfungsi sebagai benteng pertahanan terhadap pembentukan kanker
Pemahaman Konsep:
1️⃣ Apa Peran Gen Supresor Tumor dalam Siklus Sel?
2️⃣ Mengapa Hipermetilasi Promoter Menonaktifkan Gen?
3️⃣ Apakah Perubahan Ini Reversibel?
4️⃣ Implikasi Terapi Epigenetik
2️⃣ Mengapa Hipermetilasi Promoter Menonaktifkan Gen?
Kasus 2: Stres Kronis dan Gangguan Kortisol
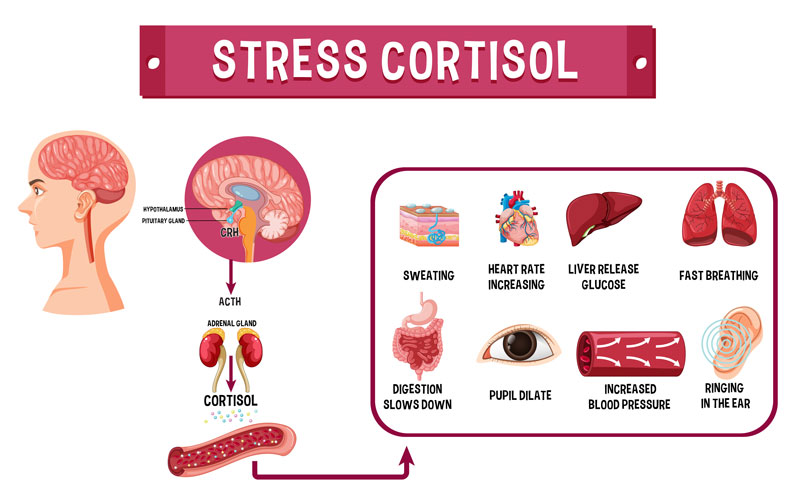
Seorang mahasiswa tingkat akhir mengalami stres akademik yang berat selama dua tahun terakhir. Ia sering mengalami kecemasan, gangguan tidur, dan mudah lelah. Pemeriksaan medis menunjukkan kadar hormon kortisol yang tidak stabil.
Hasil analisis molekuler menunjukkan adanya peningkatan metilasi pada promoter gen reseptor glukokortikoid, yaitu NR3C1. Tidak ditemukan mutasi pada gen tersebut, tetapi ekspresinya menurun.
Dokter menduga bahwa stres kronis menyebabkan perubahan epigenetik yang memengaruhi regulasi sistem stres tubuh.
Konsep Dasar:
NR3C1 (Reseptor Nuklir Subfamili 3 Grup C Anggota 1)
mengkode reseptor glukokortikoid (GR) manusia, protein penting yang mengikat kortisol dan mengatur ekspresi gen, respons inflamasi, dan metabolisme.Terletak pada kromosom 5, gen ini sangat penting untuk respons terhadap stres dan terkait dengan penyakit seperti sindrom Cushing, resistensi glukokortikoid umum, dan gangguan kesehatan mental.
Aspek-Aspek Utama NR3C1 :
- Fungsi: Setelah mengikat kortisol, GR berpindah ke nukleus untuk bertindak sebagai faktor transkripsi, mengikat Elemen Respons Glukokortikoid (GRE) untuk memodulasi ekspresi gen.
- Kaitan dengan Penyakit: Mutasi atau disregulasi dikaitkan dengan resistensi glukokortikoid umum, sindrom ovarium polikistik, obesitas, diabetes tipe 2, dan depresi.
- Epigenetika & Trauma: Pengalaman buruk di awal kehidupan dan stres kronis dapat menyebabkan perubahan metilasi pada promotor NR3C1 (khususnya ekson 1F), mengurangi ekspresi GR dan mengubah reaktivitas stres.
- Biomarker Kesehatan Mental: Studi menunjukkan bahwa tingkat ekspresi mRNA NR3C1 dalam darah perifer dapat berfungsi sebagai biomarker potensial untuk PTSD dan gangguan terkait stres.
- Struktur: Gen ini mengandung 17 ekson, termasuk sembilan ekson pertama non-pengkodean (AJ, tidak termasuk G) yang bertindak sebagai promotor alternatif.
Pemahaman Konsep:
1️⃣ Bagaimana Sistem Stres Bekerja?
2️⃣ Peran Gen Reseptor Glukokortikoid (NR3C1)
3️⃣ Apa yang Terjadi pada Stres Kronis?
4️⃣ Mengapa Metilasi Dapat Terjadi Akibat Stres?
Kasus 3: Respons Imun dan Histone Acetylation
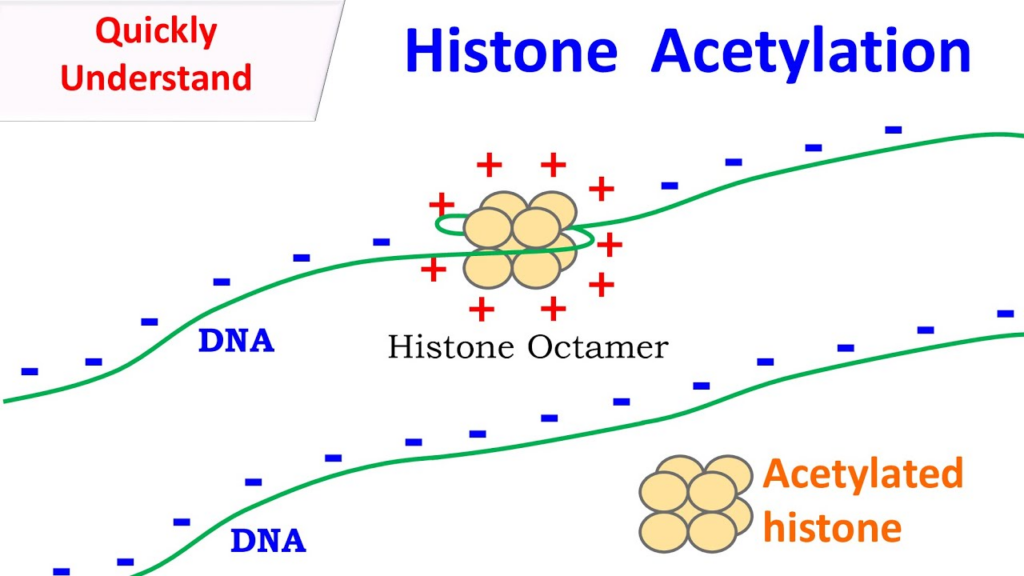
Seorang mahasiswa mengalami infeksi bakteri saluran pernapasan. Ketika diperiksa, kadar sitokin proinflamasi dalam darah meningkat. Analisis molekuler pada sel imun menunjukkan peningkatan asetilasi histon pada daerah promoter gen sitokin, khususnya gen IL6.
Tidak ditemukan mutasi pada gen tersebut. Namun, ekspresi gen IL6 meningkat secara signifikan selama infeksi berlangsung.
Peneliti menyimpulkan bahwa peningkatan ekspresi gen tersebut terjadi akibat perubahan epigenetik berupa histone acetylation.
Konsep Dasar:
Gen IL6 (Interleukin 6) mengodekan sitokin yang memiliki peran ganda, namun dalam konteks kanker lebih sering dikaitkan dengan promosi tumor (onkogenik) dan peradangan.
Fungsi Utama Gen IL6
- Regulator Inflamasi: IL6 adalah sitokin pro-inflamasi utama yang dilepaskan sebagai respons terhadap infeksi atau cedera jaringan untuk memicu pertahanan tubuh.
- Imunitas: Membantu pematangan sel B menjadi sel plasma penghasil antibodi dan mengatur diferensiasi sel T.
- Respons Fase Akut: Merangsang hati untuk memproduksi protein fase akut (seperti CRP) dan dapat menyebabkan demam.
Pemahaman Konsep:
1️⃣ Bagaimana Respons Imun Terjadi?
2️⃣ Apa Itu Histone Acetylation?
3️⃣ Apa yang Terjadi pada Kasus Ini?
4️⃣ Mengapa Mekanisme Ini Penting?
5️⃣ Apa yang Terjadi Jika Regulasi Tidak Terkontrol?
Kasus 4 : Obesitas dan Regulasi Gen Metabolisme

Seorang mahasiswa berusia 21 tahun mengalami peningkatan berat badan yang signifikan selama dua tahun terakhir. Pola makannya tinggi lemak dan gula, serta jarang berolahraga.
Pemeriksaan laboratorium menunjukkan peningkatan kadar trigliserida dan resistensi insulin ringan. Analisis molekuler menunjukkan adanya peningkatan metilasi pada promoter gen yang berperan dalam oksidasi lemak, yaitu PPARGC1A.
Tidak ditemukan mutasi pada gen tersebut, tetapi ekspresinya menurun dibandingkan individu dengan berat badan normal.
Dokter menduga pola makan dan gaya hidup memicu perubahan epigenetik yang memengaruhi regulasi gen metabolisme.
Konsep Dasar:
Pemahaman Konsep:
1️⃣ Peran Gen dalam Metabolisme Energi
2️⃣ Apa yang Terjadi pada Kasus Ini?
3️⃣ Mengapa Lingkungan Bisa Mempengaruhi Ekspresi Gen?
4️⃣ Apakah Perubahan Ini Reversibel?
Kasus 5 : Paparan Polusi dan miRNA

Seorang individu yang tinggal di daerah industri selama lebih dari 10 tahun sering mengalami gangguan pernapasan ringan dan mudah lelah. Pemeriksaan menunjukkan adanya peningkatan stres oksidatif dan inflamasi kronis tingkat rendah.
Analisis molekuler menunjukkan perubahan ekspresi beberapa microRNA (miRNA), terutama peningkatan ekspresi miR-21, yang diketahui berperan dalam regulasi gen inflamasi dan apoptosis.
Tidak ditemukan mutasi pada gen target. Namun, terjadi penurunan ekspresi beberapa gen antiinflamasi akibat peningkatan miR-21.
Peneliti menyimpulkan bahwa paparan polusi udara memengaruhi regulasi ekspresi gen melalui mekanisme miRNA.
Konsep dasar:
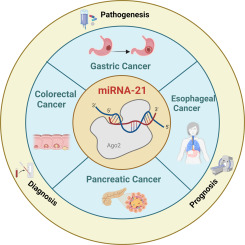
miR-21 (microRNA-21) adalah salah satu jenis mikroRNA yang paling awal diidentifikasi dan paling banyak dipelajari karena perannya yang sangat dominan sebagai oncomiR (mikroRNA yang bersifat onkogenik atau pemicu kanker). Berbeda dengan p16 yang merupakan “rem” sel, miR-21 justru sering kali “melepaskan rem” tersebut dengan menghambat protein supresor tumor
Mekanisme Kerja sebagai OncomiR
miR-21 bekerja pada tingkat pasca-transkripsi dengan mengikat mRNA dari gen target, sehingga mencegah pembentukan protein supresor tumor yang penting. Target utamanya meliputi:
- PTEN: miR-21 menghambat PTEN, sebuah pengatur kunci jalur PI3K/Akt. Tanpa PTEN, sel akan terus membelah dan bertahan hidup secara abnormal.
- PDCD4 (Programmed Cell Death Protein 4): Dengan menekan protein ini, miR-21 membantu sel kanker menghindari kematian sel (apoptosis) dan meningkatkan kemampuan invasi sel ke jaringan lain.
- TPM1 (Tropomyosin 1): Menghambat protein ini berkontribusi pada kemampuan sel kanker untuk bermigrasi dan menyebar (metastasis)
Karakteristik dalam Kanker
- Ekspresi Berlebih (Overexpression): miR-21 ditemukan meningkat pada hampir semua jenis kanker padat pada manusia, termasuk kanker payudara, paru-paru, usus besar, pankreas, dan glioblastoma.
- Biomarker Prognostik: Kadar miR-21 yang tinggi dalam jaringan tumor atau darah (serum) sering dikaitkan dengan prognosis yang buruk, stadium penyakit yang lebih lanjut, dan tingkat kelangsungan hidup yang lebih rendah.
- Resistensi Terapi: Peningkatan miR-21 juga berperan dalam membuat sel kanker menjadi kebal (resisten) terhadap kemoterapi dan radioterapi.
Tugas:
1️⃣ Apa Itu miRNA?
2️⃣ Bagaimana Polusi Dapat Mempengaruhi miRNA?
3️⃣ Mengapa Ini Termasuk Regulasi Ekspresi Gen?
4️⃣ Apa Dampaknya bagi Kesehatan?
Kasus 6 : Nutrisi Prenatal dan Pemrograman Epigenetik
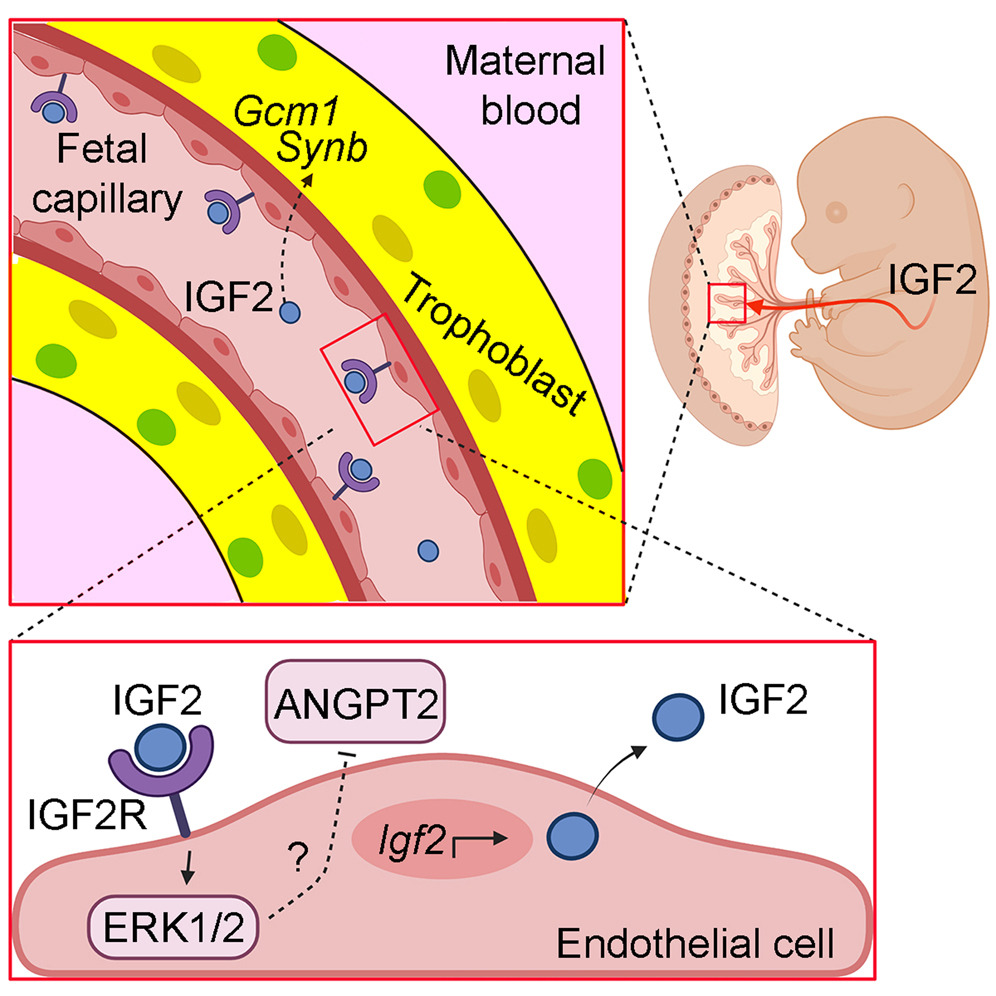
Seorang ibu mengalami kekurangan asupan protein dan asam folat selama trimester pertama kehamilan. Bayi yang dilahirkan memiliki berat badan rendah. Saat remaja, anak tersebut menunjukkan kecenderungan obesitas dan resistensi insulin.
Analisis molekuler menunjukkan perubahan pola metilasi pada gen yang mengatur pertumbuhan dan metabolisme, salah satunya IGF2.
Tidak ditemukan mutasi pada gen tersebut. Namun, terjadi perubahan tingkat ekspresi akibat perbedaan pola metilasi DNA dibandingkan individu yang mendapat nutrisi prenatal optimal.
Peneliti menyimpulkan bahwa kondisi nutrisi selama kehamilan memengaruhi regulasi ekspresi gen jangka panjang melalui mekanisme epigenetik.
Konsep Dasar:
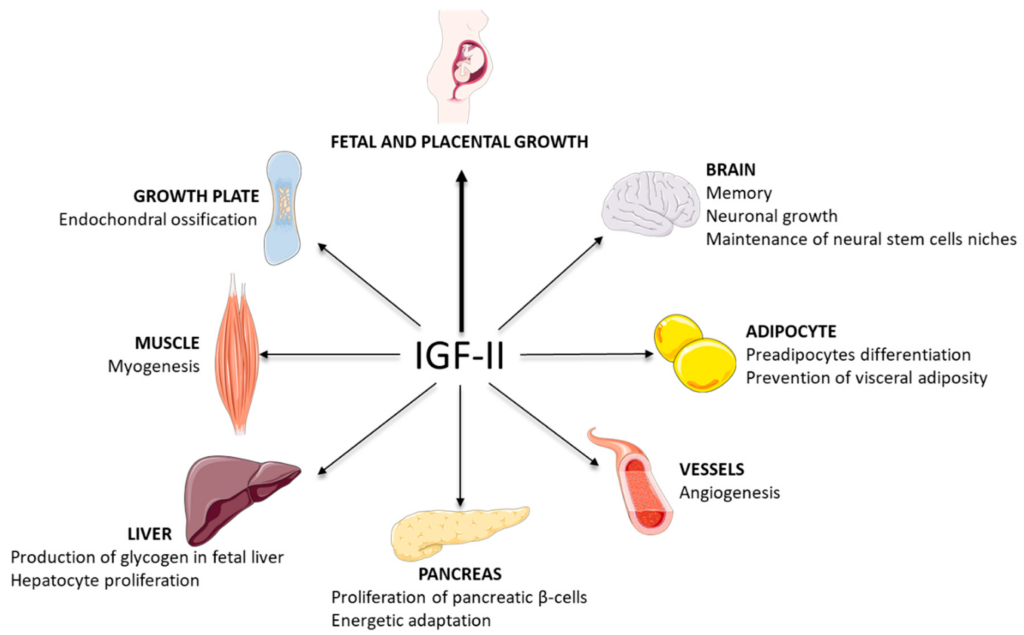
Gen IGF2 (Insulin-like Growth Factor 2) adalah gen yang mengodekan protein hormon yang sangat krusial dalam pertumbuhan dan perkembangan janin. Berbeda dengan p16 atau miR-21 yang telah dibahas sebelumnya, IGF2 sering kali bertindak sebagai onkogen (pemicu kanker) ketika ekspresinya berlebihan.
Karakteristik Unik: Imprinting Genomik
IGF2 adalah salah satu dari sedikit gen manusia yang memiliki sifat imprinting genomik:
- Hanya Satu Salinan Aktif: Dalam kondisi normal, hanya salinan gen yang diwarisi dari ayah (paternal) yang aktif, sementara salinan dari ibu (maternal) dibungkam.
- Loss of Imprinting (LOI): Pada banyak jenis kanker, terjadi kegagalan sistem ini sehingga kedua salinan gen (dari ayah dan ibu) menjadi aktif. Fenomena ini menyebabkan produksi protein IGF2 melonjak drastis, yang memicu pembelahan sel yang tidak terkendali.
Pemahaman Konsep:
1️⃣ Apa Itu Pemrograman Epigenetik?
2️⃣ Peran Gen IGF2
3️⃣ Bagaimana Nutrisi Mempengaruhi Metilasi DNA?
4️⃣ Mengapa Dampaknya Baru Terlihat Saat Dewasa?
Studi Kasus Materi 2
- Kasus 1
- Kasus 2
- Kasus 3
- Kasus 4
- Kasus 5
- Kasus 6
Kasus 1
“ISU KANKER DAN KAITANNYA DENGAN KONTROL GENETIK”
Berdasarkan data Global Cancer Statistics (2020), kanker payudara paling banyak didiagnosis pada perempuan. Penyakit kanker payudara dipicu oleh faktor lingkungan, seperti: merokok, diet, atau polutan kimia yang menyebabkan mutasi pada gen Breast Cancer-
1 (BRCA-1). Faktor lingkungan tersebut dapat memicu perubahan materi genetik sehingga menganggu pembelahan sel. Di Jawa Timur, kanker payudara memiliki angka kejadian yang tinggi. Bertepatan dengan Hari Kanker Sedunia, RS Onkologi Surabaya dan Puteri Indonesia Jawa Timur 2022 mendukung program pemerintah dalam mewujudkan Indonesia Bebas Kanker Payudara Stadium Lanjut 2035, dengan mengadakan deteksi dini DNA fungsional biomarker kanker payudara. Akan tetapi, konsekuensi deteksi kanker payudara menyebabkan tenaga medis dapat mengetahui privasi informasi genetik individu.
Peneliti kanker berusaha mengidentifikasi penyebab kanker secara genetik. Peneliti kanker telah mengidentifikasi dua kelompok gen yang ketika bermutasi berkontribusi pada perkembangan kanker, yaitu proto-oncogenes dan tumor suppressor genes. Dalam keadaan normal, ekspresi tumor suppressor genes dapat mengatur pembelahan sel secara stabil. Namun, ketika tumor suppressor genes termutasi, maka ekspresinya menyebabkan pembelahan sel yang tidak terkendali. Seseorang X didiagnosis dokter terkena kanker payudara stadium akhir.
Hasil deteksi menunjukkan bahwa sel kanker telah membelah tanpa henti hingga membentuk tumor dan bermetastasis dengan menyebar ke jaringan di sekitarnya.
Deteksi awal kanker payudara penting dilakukan untuk mengurangi angka kasus kematian. Hasil penelitian tahun 1895, menunjukkan metode sinar-X dosis rendah dapat digunakan untuk deteksi awal kanker payudara. Namun, hasilnya kurang sensitif karena jaringan payudara yang padat. Lebih lanjut, hasil penelitian tahun 1997 deteksi awal kanker payudara menggunakan uji sampel darah. Hasilnya, sensitif dalam mendeteksi gen BRCA1. Terapi gen merupakan transfer materi genetik yang berfungsi untuk menyembuhkan penyakit, contohnya viroterapi onkolitik untuk terapi kanker payudara. Peneliti mengklaim bahwa viroterapi onkolitik bekerja dengan mentransfer virus tertentu untuk menyerang sel-sel kanker yang sangat aktif membelah.
Apabila ditinjau dari mekanisme replikasi virus, adavirus yang bereplikasi dengan siklus litik dan virus yang bereplikasi dengan siklus lisogenik.
Virus yang bereplikasi dengan siklus litik, maka di akhir siklusnya dapat mematikan sel kanker, sedangkan virus bereplikasi dengan siklus lisogenik, maka di akhir siklusnya dapat memicu penggandaan materi genetik virus dan sel kanker.
Sumber Diadaptasi dari: Nounou, M. I., ElAmrawy, F., Ahmed, N., Abdelraouf, K., Goda, S.,
& Syed-Sha-Qhattal, H. (2015). Breast Cancer: Conventional Diagnosis and Treatment
Modalities and Recent Patents and Technologies. Breast Cancer: Basic and Clinical Research, 9s2,
BCBCR.S29420. https://doi.org/10.4137/bcbcr.s29420
Kasus 2
ISU LEUKEMIA DAN KAITANNYA DENGAN KONTROL GENETIK PEMBELAHAN SEL IMUN
Berdasarkan laporan World Health Organization tahun 2022, leukemia merupakan salah satu kanker darah yang banyak ditemukan pada anak dan remaja. Leukemia terjadi akibat gangguan pada sel punca hematopoietik di sumsum tulang yang menyebabkan produksi sel imun tidak terkendali. Pada kondisi normal, pembelahan sel imun dikontrol oleh berbagai gen pengatur siklus sel seperti gen p53 dan gen pengatur apoptosis.
Beberapa faktor lingkungan seperti paparan radiasi, bahan kimia berbahaya, atau mutasi genetik dapat menyebabkan perubahan pada materi genetik sel darah. Mutasi tersebut dapat mengubah proto-oncogenes menjadi oncogenes atau menonaktifkan tumor suppressor genes sehingga pembelahan sel menjadi tidak terkendali. Akibatnya, sel darah putih yang abnormal akan terus membelah dan menumpuk dalam sumsum tulang.
Seorang pasien remaja berinisial A mengalami gejala lemas, pucat, dan sering mengalami infeksi. Setelah dilakukan pemeriksaan darah dan biopsi sumsum tulang, dokter mendiagnosis pasien tersebut menderita leukemia limfoblastik akut. Hasil pemeriksaan menunjukkan bahwa sel imun abnormal terus membelah tanpa kontrol sehingga menghambat produksi sel darah normal.
Selain mutasi genetik, penelitian terbaru menunjukkan bahwa perubahan epigenetik seperti metilasi DNA juga dapat memengaruhi ekspresi gen yang mengatur siklus sel. Perubahan epigenetik tersebut dapat menyebabkan gen penghambat tumor tidak aktif sehingga mempercepat perkembangan kanker darah.
Berbagai terapi sedang dikembangkan untuk mengatasi leukemia, seperti kemoterapi, terapi target molekuler, serta imunoterapi yang memanfaatkan kemampuan sel imun untuk mengenali dan menghancurkan sel kanker.
Sumber rujukan:
- World Health Organization. (2023). Cancer fact sheets: Leukemia.
- Francesco Lanza & Sucai Bi. (1995). Role of p53 in leukemogenesis of chronic myeloid leukemia. Stem Cells, 13(4), 445–452.
- National Cancer Institute. (2022). Leukemia—Patient Version.
- Marwan Kwok et al. (2021). Targeting the p53 pathway in chronic lymphocytic leukemia. Cancers, 13(18), 4681.
Kasus 3
PERBEDAAN EKSPRESI GEN PADA KEMBAR IDENTIK DAN KAITANNYA DENGAN KONTROL PEMBELAHAN SEL

Berdasarkan penelitian di bidang Epigenetics, individu yang memiliki urutan DNA yang sama belum tentu menunjukkan kondisi kesehatan yang sama. Hal ini dapat terjadi karena adanya perbedaan dalam regulasi ekspresi gen yang dipengaruhi oleh faktor lingkungan, gaya hidup, maupun perubahan epigenetik.
Dua saudara kembar identik diketahui memiliki urutan DNA yang hampir sama karena berasal dari satu zigot yang membelah menjadi dua embrio. Secara genetik, keduanya memiliki potensi biologis yang sama, termasuk gen yang mengatur pembelahan sel dan sistem imun. Namun, pada usia 45 tahun salah satu dari saudara kembar tersebut didiagnosis mengalami Colorectal Cancer, sedangkan saudara lainnya tetap sehat tanpa gejala penyakit.
Hasil pemeriksaan genetik menunjukkan bahwa tidak terdapat mutasi DNA yang signifikan pada gen pengatur siklus sel pada kedua individu tersebut. Namun, analisis ekspresi gen menunjukkan adanya perbedaan pada gen yang mengatur checkpoint siklus sel, khususnya pada fase G1/S. Checkpoint G1/S merupakan tahap penting dalam siklus sel yang menentukan apakah sel akan melanjutkan proses replikasi DNA atau menghentikan pembelahan apabila terjadi kerusakan pada materi genetik.
Penelitian lebih lanjut menunjukkan bahwa pada individu yang mengalami kanker, beberapa gen penghambat tumor mengalami penurunan ekspresi akibat perubahan epigenetik seperti metilasi DNA dan modifikasi histon. Perubahan tersebut menyebabkan gen yang berfungsi menghambat pembelahan sel tidak aktif secara optimal. Akibatnya, sel dapat melewati checkpoint siklus sel tanpa kontrol yang ketat sehingga terjadi proliferasi sel yang tidak terkendali dan akhirnya membentuk tumor.
Selain faktor epigenetik, gaya hidup seperti pola makan, paparan polutan, tingkat stres, dan aktivitas fisik juga dapat memengaruhi regulasi ekspresi gen. Faktor-faktor lingkungan tersebut dapat memicu perubahan epigenetik yang berbeda pada masing-masing individu meskipun memiliki materi genetik yang sama.
Kasus ini menunjukkan bahwa perkembangan kanker tidak hanya dipengaruhi oleh mutasi genetik, tetapi juga oleh mekanisme regulasi gen yang bersifat epigenetik. Oleh karena itu, penelitian mengenai epigenetika menjadi penting untuk memahami bagaimana faktor lingkungan dapat memengaruhi ekspresi gen yang mengontrol pembelahan sel serta meningkatkan risiko terjadinya kanker.
Sumber:
Diadaptasi dari Fraga, M. F., et al. (2005). Epigenetic differences arise during the lifetime of monozygotic twins. Proceedings of the National Academy of Sciences; Hanahan, D., & Weinberg, R. (2011). Hallmarks of Cancer: The Next Generation. Cell; National Cancer Institute.
Kasus 4
GANGGUAN FUNGSI SEL BETA PANKREAS DAN KAITANNYA DENGAN KONTROL PEMBELAHAN SEL
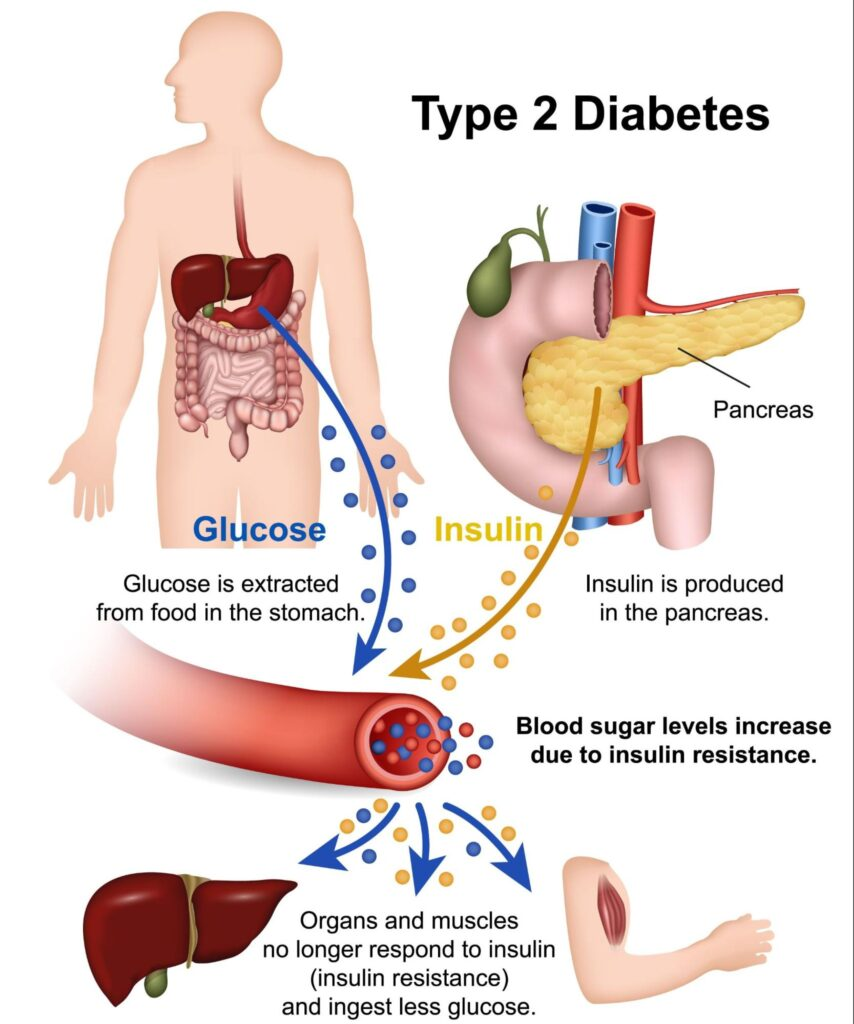
Menurut laporan World Health Organization, jumlah penderita Type 2 Diabetes terus meningkat di berbagai negara akibat perubahan gaya hidup, pola makan tinggi kalori, serta kurangnya aktivitas fisik. Diabetes tipe-2 merupakan penyakit metabolik yang ditandai oleh peningkatan kadar glukosa darah akibat resistensi insulin dan gangguan fungsi sel beta pankreas.
Sel beta pankreas merupakan sel yang terdapat pada pulau Langerhans dan berfungsi memproduksi hormon insulin. Dalam kondisi normal, sel beta memiliki kemampuan untuk mempertahankan jumlah sel melalui proses proliferasi yang dikontrol oleh mekanisme siklus sel. Proses pembelahan sel ini diatur oleh berbagai gen pengontrol siklus sel, termasuk gen yang mengatur checkpoint siklus sel serta protein regulator seperti cyclin dan cyclin-dependent kinase.
Pada penderita diabetes tipe-2, berbagai penelitian menunjukkan adanya stres metabolik kronis yang disebabkan oleh hiperglikemia berkepanjangan, peningkatan asam lemak bebas, serta inflamasi sistemik. Kondisi ini dapat memicu kerusakan sel beta pankreas melalui beberapa mekanisme biologis. Salah satunya adalah penurunan kemampuan proliferasi sel beta sehingga jumlah sel yang memproduksi insulin semakin berkurang.
Selain itu, stres metabolik juga dapat meningkatkan proses apoptosis atau kematian sel terprogram pada sel beta pankreas. Aktivasi jalur inflamasi dan stres oksidatif menyebabkan perubahan ekspresi gen yang berperan dalam regulasi siklus sel dan mekanisme kelangsungan hidup sel. Akibatnya, keseimbangan antara proliferasi sel dan kematian sel menjadi terganggu.
Penelitian juga menunjukkan bahwa resistensi insulin pada jaringan tubuh dapat memperparah kondisi tersebut. Ketika jaringan tubuh tidak merespons insulin secara optimal, pankreas akan berusaha meningkatkan produksi insulin untuk mempertahankan kadar glukosa darah tetap normal. Namun, kerja berlebihan pada sel beta dalam jangka panjang justru dapat mempercepat kerusakan sel dan menurunkan kapasitas regenerasi sel beta.
Beberapa studi terbaru menunjukkan bahwa faktor epigenetik, seperti perubahan metilasi DNA dan modifikasi histon, juga dapat memengaruhi ekspresi gen yang mengatur proliferasi dan diferensiasi sel beta pankreas. Perubahan epigenetik ini dapat dipicu oleh faktor lingkungan seperti pola makan tidak sehat, obesitas, dan stres metabolik berkepanjangan.
Kasus ini menunjukkan bahwa perkembangan diabetes tipe-2 tidak hanya berkaitan dengan gangguan metabolisme glukosa, tetapi juga melibatkan perubahan pada mekanisme kontrol pembelahan sel dan kelangsungan hidup sel beta pankreas. Pemahaman mengenai regulasi siklus sel pada sel beta diharapkan dapat membantu pengembangan terapi baru yang bertujuan meningkatkan regenerasi sel beta dan memperbaiki fungsi pankreas pada penderita diabetes.
Sumber:
Diadaptasi dari Butler, A. E., et al. (2003). Beta-cell deficit and increased beta-cell apoptosis in humans with type 2 diabetes. Diabetes; Donath, M. Y., & Halban, P. A. (2004). Decreased beta-cell mass in diabetes: significance, mechanisms and therapeutic implications. Diabetologia; International Diabetes Federation.
Kasus 5
ISU KANKER SERVIKS DAN PERAN VIRUS DALAM KONTROL PEMBELAHAN SEL
Kanker serviks merupakan salah satu kanker yang banyak menyerang perempuan di negara berkembang. Berdasarkan laporan International Agency for Research on Cancer, sebagian besar kasus kanker serviks disebabkan oleh infeksi virus HPV (Human Papillomavirus).
Virus HPV dapat memasukkan materi genetiknya ke dalam sel inang sehingga mengganggu regulasi siklus sel. Protein virus tertentu dapat menonaktifkan gen tumor suppressor seperti p53 dan Rb yang berfungsi mengontrol pembelahan sel.
Seorang pasien perempuan berusia 40 tahun mengalami perdarahan abnormal dan setelah pemeriksaan lanjutan didiagnosis menderita kanker serviks. Hasil analisis molekuler menunjukkan bahwa DNA virus HPV telah terintegrasi ke dalam genom sel serviks.
Selain mutasi genetik, infeksi virus juga dapat memicu perubahan epigenetik seperti metilasi DNA yang memengaruhi ekspresi gen pengatur pertumbuhan sel. Perubahan tersebut dapat mempercepat perkembangan kanker.
Upaya pencegahan kanker serviks dapat dilakukan melalui vaksinasi HPV, skrining rutin, serta edukasi kesehatan reproduksi.
Sumber rujukan:
Stephen B. Baylin & Peter A. Jones. (2016). Epigenetic determinants of cancer. Cold Spring Harbor Perspectives in Biology.
World Health Organization. (2022). Cervical cancer.
Harald zur Hausen. (2009). Papillomaviruses in the causation of human cancers. Virology.
International Agency for Research on Cancer. (2020). HPV and cervical cancer.
Kasus 6
ISU PENYAKIT AUTOIMUN DAN KAITANNYA DENGAN KONTROL GENETIK RESPON IMUN
Penyakit autoimun merupakan kondisi ketika sistem imun tubuh menyerang sel dan jaringan tubuh sendiri karena gagal mengenali antigen sebagai bagian dari diri (self). Secara normal, sistem imun memiliki mekanisme toleransi imun yang berfungsi mencegah limfosit menyerang jaringan tubuh. Namun pada kondisi tertentu, mekanisme ini dapat terganggu sehingga menyebabkan aktivasi sel imun secara abnormal.
Salah satu contoh penyakit autoimun adalah Systemic Lupus Erythematosus (SLE) yang ditandai dengan produksi antibodi terhadap komponen inti sel, seperti DNA dan protein nuklear. Penyakit ini sering ditemukan pada perempuan usia produktif dan dapat menyerang berbagai organ, seperti kulit, ginjal, sendi, dan sistem saraf.
Penelitian menunjukkan bahwa penyakit autoimun tidak hanya dipengaruhi oleh faktor lingkungan, tetapi juga oleh faktor genetik yang mengatur fungsi sistem imun. Beberapa gen yang terlibat dalam regulasi respon imun, seperti gen pada Human Leukocyte Antigen (HLA) dan gen yang mengatur aktivasi limfosit T dan limfosit B, diketahui memiliki hubungan dengan peningkatan risiko penyakit autoimun. Mutasi atau perubahan regulasi ekspresi gen tersebut dapat menyebabkan aktivasi sel imun yang berlebihan.
Dalam kondisi normal, limfosit yang mengenali antigen diri akan dieliminasi melalui proses seleksi selama perkembangan sel imun di organ limfoid. Namun pada penderita penyakit autoimun, proses seleksi tersebut tidak berjalan sempurna sehingga sel imun autoreaktif dapat tetap bertahan dan berkembang biak melalui proses proliferasi sel.
Selain itu, gangguan pada mekanisme apoptosis juga dapat berperan dalam perkembangan penyakit autoimun. Sel yang seharusnya mengalami kematian terprogram dapat bertahan lebih lama dan memicu respon imun terhadap komponen sel yang dilepaskan selama proses kerusakan jaringan. Hal ini menyebabkan terjadinya peradangan kronis yang merusak jaringan tubuh.
Seorang pasien perempuan berusia 30 tahun datang ke rumah sakit dengan keluhan nyeri sendi, ruam pada wajah berbentuk seperti kupu-kupu, serta kelelahan yang berkepanjangan. Hasil pemeriksaan laboratorium menunjukkan adanya antibodi anti-DNA dalam darah serta peningkatan aktivitas limfosit B. Dokter kemudian mendiagnosis pasien tersebut menderita penyakit autoimun yang berkaitan dengan gangguan regulasi respon imun.
Penelitian lebih lanjut menunjukkan bahwa pada pasien tersebut terjadi perubahan regulasi ekspresi gen yang mengatur aktivasi dan proliferasi limfosit. Akibatnya, sel-sel imun terus berkembang dan menghasilkan antibodi yang menyerang jaringan tubuh sendiri. Kondisi ini menunjukkan bahwa gangguan pada kontrol genetik sistem imun dapat memicu terjadinya penyakit autoimun.
Oleh karena itu, pemahaman mengenai mekanisme genetik yang mengatur respon imun sangat penting untuk mengembangkan strategi terapi yang lebih efektif. Beberapa pendekatan terapi yang sedang dikembangkan meliputi penggunaan obat imunosupresan, terapi antibodi monoklonal, serta terapi yang menargetkan jalur molekuler yang mengatur aktivasi sel imun.
Sumber Rujukan
- Tsokos, G. C. (2011). Systemic lupus erythematosus. New England Journal of Medicine, 365(22), 2110–2121.
- Abbas, A. K., Lichtman, A. H., & Pillai, S. (2021). Cellular and Molecular Immunology (10th ed.). Elsevier.
- Davidson, A., & Diamond, B. (2001). Autoimmune diseases. New England Journal of Medicine, 345(5), 340–350.
